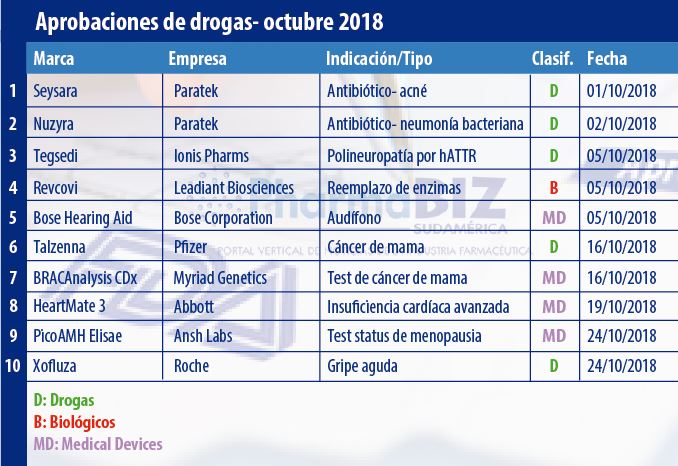
Durante el décimo mes del año la FDA le dio el visto bueno a por lo menos cinco medicamentos, cuatro medical devices y a un biológico. Por caso resaltó la norteamericana Pfizer que recibió el aval para su oncológico Talzenna. El mismo está indicado para el cáncer de mama tipo HER2 negativo avanzado o metastásico.
Pharmabiz realizó un relevamiento de las aprobaciones más destacadas otorgadas por la FDA durante el mes de octubre.
Entre las compañías que obtuvieron el visto bueno del organismo resaltó la norteamericana Pfizer, que recibió el pulgar arriba para su oncológico Talzenna. El mismo está indicado para el cáncer de mama tipo HER2 negativo avanzado o metastásico. En simultáneo la agencia aprobó el test BRACAnalysis CDx, para ser utilizado en conjunto para identificar personas con este tipo de cáncer que son elegibles para el uso de Talzenna. El mismo pertenece a la también norteamericana Myriad Genetics. Ver artículo.
La suiza Roche fue otra que consiguió un OK de la FDA. Fue para Xofluza, un antigripal de última generación que se espera que sea el segundo producto que siga la saga de Tamiflu. Aunque su tecnología es totalmente diferente ya que funciona con una sola dosis. Ver artículo.
En materia de tecnología médica la agencia regulatoria le levantó el pulgar a un test de diagnóstico que opera como una herramienta para determinar el estado menopáusico. Se trata de PicoAMH Elisa, el que está bajo el ala de la norteamericana Ansh Labs.
La agencia regulatoria también avaló dos medicamentos de la norteamericana Paratek. Por un lado aprobó a Seysara, indicado para lesiones inflamatorias en personas con acné vulgar no nodular de moderado a severo. A su vez le levantó el pulgar a Nuzyra, un antibiótico para el tratamiento de adultos con neumonía bacteriana, y para infecciones agudas de la piel. Ver artículo. Ver artículo.
Por otro lado, la FDA le dio luz verde a Tegsedi que lleva el sello de la biofarmacéutica Ionis en conjunto con su subsidiaria, la norteamericana Akcea. El mismo fue aprobado para una enfermedad genética rara: la polineuropatía causada por amiloidosis mediada por transtiretina hereditaria, hATTR, en adultos. Ver artículo.
La norteamericana Paratek obtuvo luz verde para dos medicamentos: Seysara y Nuzyra. El primero está indicado para lesiones inflamatorias en personas con acné vulgar no nodular. Mientras que el segundo fue avalado para adultos con neumonía bacteriana.
Otra que consiguió el visto bueno del organismo fue la norteamericana Lediant Biosciences, para su biológico inyectable recombinante Revcovi. Se trata de una terapia de reemplazo de enzimas para el tratamiento de un trastorno genético grave bautizado ADA-SCID. Ver press release.
En materia de medical devices la que se destacó fue la norteamericana Abbott, que consiguió luz verde para su producto HeartMate 3. Se trata de un dispositivo de asistencia ventricular izquierda para personas con insuficiencia cardíaca avanzada. Ver press release.
Asimismo, la FDA le levantó el pulgar al audífono Bose Hearing Aid, respaldado por la norteamericana Bose Corporation. Además, le dio el OK al device PicoAMH Elisa, un test de diagnóstico que ayuda en la determinación del estado menopáusico. El mismo está bajo el ala de la también norteamericana Ansh Labs. Ver press release.