Cada 17 de noviembre, el cáncer de pulmón queda en primer plano. En el marco del Día Internacional de la lucha contra esta enfermedad, fecha instaurada por la Organización Mundial de la Salud, Pharmabiz pasa revista a los tratamientos aprobados en la Argentina.
El segmento de Onco está en el foco de gran parte de las multis de farma. Y específicamente en el nicho del cáncer de plumón, las compañías avanzan en tratamientos cada vez más específicos.
En este marco, en el Día Internacional de la Lucha Contra el Cáncer de Pulmón, instaurado por la Organización Mundial de la Salud, OMS, Pharmabiz recapitula los medicamentos que ya cuentan con el aval de la ANMAT para esta indicación.
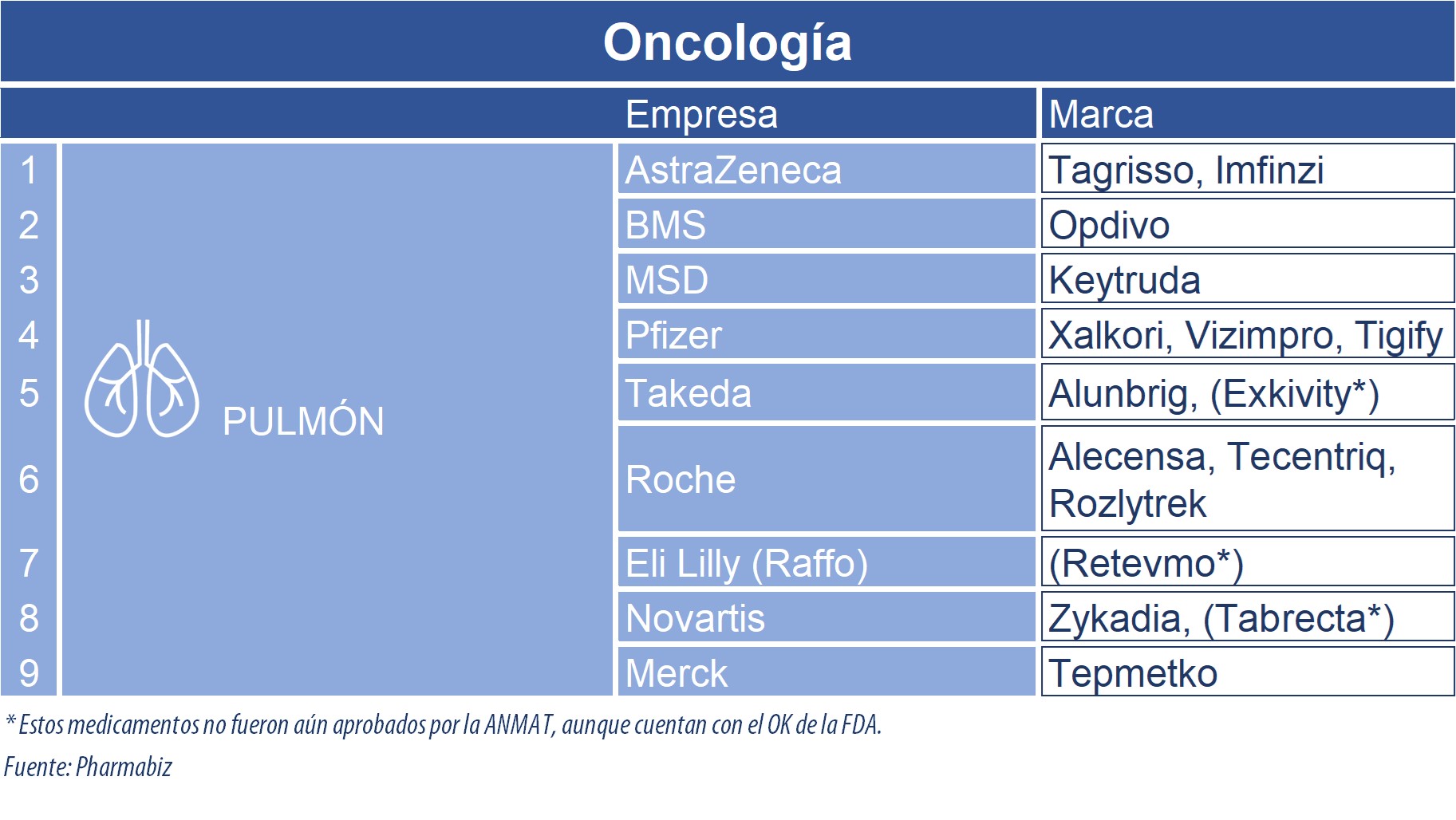
En el mercado local, se destaca la norteamericana Pfizer con una tríada de oncológicos, para distintas formas de cáncer de pulmón inducido por mutaciones genéticas. El primero que recibió el OK fue Xalkori; y luego, en 2020, Vizimpro y Tigify. También resalta la suiza Roche con Alecensa, Tecentriq y Rozlytrek, su terapia tumoral agnóstica, la que obtuvo la autorización bajo condiciones especiales para ser inscripta en el Registro de Especialidades Medicinales en abril de este año.
Otra que figura entre los competidores es la británica AstraZeneca, con una dupla de biológicos: Tagrisso e Imfinzi. El listado se completa con la estadounidense BMS, que cuenta con Opdivo; la japonesa Takeda, que dispone de Alunbrig; la norteamericana MSD, que tiene en su portafolio a Keytruda; y la suiza Novartis, que tiene a Zykadia.
A su vez, es relevante mencionar la aprobación de Tepmetko de la alemana Merck por parte de la ANMAT. El mismo está indicado para cáncer de pulmón no microcítico metastásico, con alteraciones por omisión del exón 14 en el gen MET.
Además, existen al menos tres productos indicados para diferentes formas de cáncer de pulmón, que aún no están disponibles en la Argentina. Se trata de Tabrecta, desarrollado por la suiza Novartis; Retevmo, de la norteamericana Eli Lilly; y Exkivity, de la japonesa Takeda.