
Argentina llegó tarde a la era de los autotests COVID-19. Mientras que en Estados Unidos hay 21 marcas autorizadas y todo arrancó en noviembre del 2020, en las farmacias locales no se registra un gran interés por parte de los consumidores. Los tironeos entre bioquímicos y farmacéuticos fueron una de las principales razones por las que en la Argentina estos devices de uso hogareño no cumplieron el rol que en el resto del mundo.
Mientras que en Estados Unidos y en otros países desarrollados los devices médicos hogareños para múltiples usos son moneda corriente, en la Argentina todo está en pañales. A nivel local tan sólo se comercializan autotests de embarazo o de ovulación.
Sin embargo en otros mercados hay pruebas de venta libre para detectar HIV; alcohol (por saliva o aliento); cannabinoides y cocaína; metabolitos; niveles en sangre de colesterol, bilirrubina y hemoglobina; e incluso de mutaciones genéticas para la determinación del cáncer de mama o de ovario; entre otros. Se trata de una amplia gama que comprende múltiples diagnósticos que en la Argentina únicamente pueden realizarse bajo el andarivel de los laboratorios bioquímicos y bajo prescripción médica. Ver tests OTC de FDA.
Aunque es importante resaltar además que la FDA distingue a una «tercera vía». Son los tests bautizados POCT –point of care testing, según las siglas en inglés-, a los que apelan los médicos y que se usan en el punto de cuidado del paciente. Así los diferencia de aquellos que requieren de equipamiento médico in situ para ser realizados; y de los autotests, que se compran directamente en un punto de venta.
Y dentro de este tercer grupo es donde están enrolados los autotests COVID-19, a los que se les dio mucha lata desde los medios masivos nacionales, pero que no registraron un gran interés por parte de los consumidores en la Argentina. Esto fue en función de varias razones. Por un lado, el engorroso trámite de tener que informar el resultado al punto de venta. Por otro, la simultánea disponibilidad de testeos gratuitos por parte del Estado. Y también en función de que la llegada tardía de estos productos se dio en paralelo con el descenso de la curva de casos.
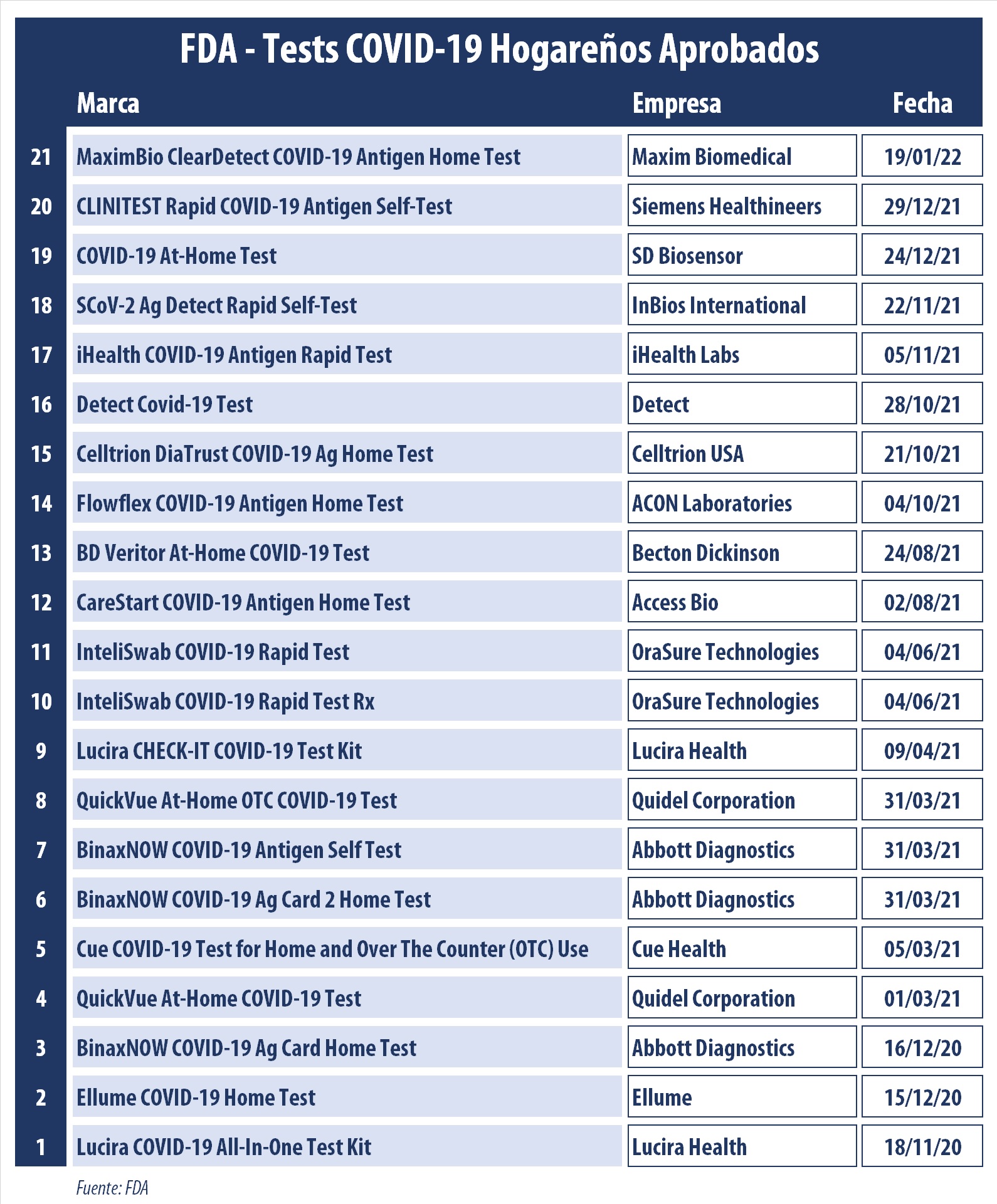
Es así que mientras en la Argentina se aprobaron cinco autotests, en los Estados Unidos ya son 21 las marcas autorizadas por la FDA. Las mismas se venden de forma masiva desde noviembre del 2020, cuando la agencia norteamericana otorgó el primer OK, y se diferencian entre 17 kits de detección de antígenos y cuatro de detección molecular (PCR). Ver listado FDA antígenos. // Ver listado FDA moleculares.
En el otro lado del hemisferio, en la Argentina, la ANMAT autorizó únicamente pruebas hogareñas de antígenos. Al momento, las marcas que obtuvieron luz verde son: SARS-CoV-2 Antigen Self Test Nasal, de la suiza Roche; Panbio, de la norteamericana Abbott; Immunobio, de origen chino e importado por la firma Vyam Group -comercializado por la nacional Grimberg Dentales– y por Laboratorios Jayor; WL Check, de la santafesina Wiener; y SARS-CoV-2 Antigen Test Kit (LFIA), otro test chino, distribuido por Asserca. Ver «ANMAT, luz verde a autotests de COVID-19».





Autotests hogareños: un informe que pone blanco sobre negro. COVID-19 y más. Hacé click. #Autotests #COVID-19 #Farmacias #FDA #ANMAT #Farma #Pharmabiz















