La FDA puso la lupa sobre los genéricos que fueron avalados durante el 2018. En su informe anual consignó que en el año que cerró le dio luz verde a 1.021 nuevas copias de medicamentos.
La FDA publicó su anuario de los genéricos que fueron aprobados por el organismo durante el 2018. Ver informe.
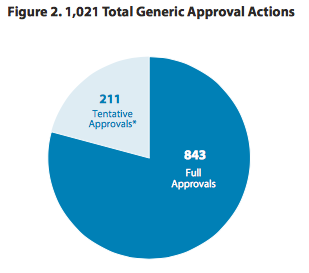
Allí la agencia regulatoria mostró que en el año que cerró le levantó el pulgar a 1.021 genéricos, de los cuales 211 obtuvieron una aprobación tentativa, la que pospone el OK final hasta tanto se resuelvan ciertos requisitos de patente o exclusividad.
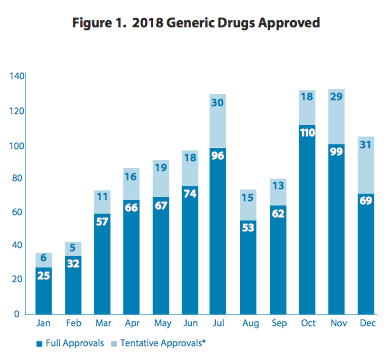
La FDA también consignó que el mayor número de aprobaciones se dio en los meses de octubre y noviembre, los que empataron con igual cifra luego de darle luz verde a 128 nuevas copias de medicamentos. En contrapartida, enero del 2018 fue el período con menos avales con tan sólo 31 OKs.
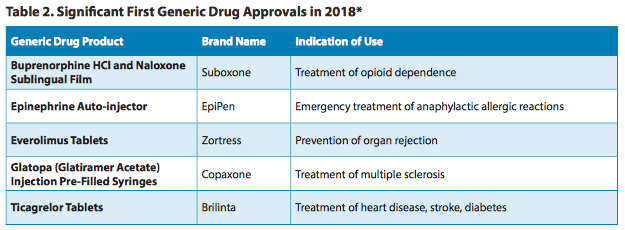
Respecto de las autorizaciones más significativas, el organismo resaltó el visto bueno que obtuvieron seis productos. Fueron las versiones genéricas de Suboxone, de la británica Indivior; EpiPen, de la norteamericana Mylan; Zortress, de la suiza Novartis; Copaxone, de la israelí Teva; y Brilinta, de la británica AstraZeneca.
La oficina de genéricos de la FDA, que está capitaneada por Kathleen Uhl, destacó a su vez que el 2018 fue el primer año en que tomó vigencia la reautorización de las enmiendas a las tarifas para usuarios de medicamentos genéricos –GDUFA II por sus siglas en inglés-.