Con abril en el retrovisor, toca repasar los movimientos de la FDA durante el mes. Hubo tanto aprobaciones novedosas como anuncios institucionales.
La FDA cerró el cuarto mes del año con novedades de todo tipo. El equipo de Pharmabiz realiza un repaso de lo que hay que saber.
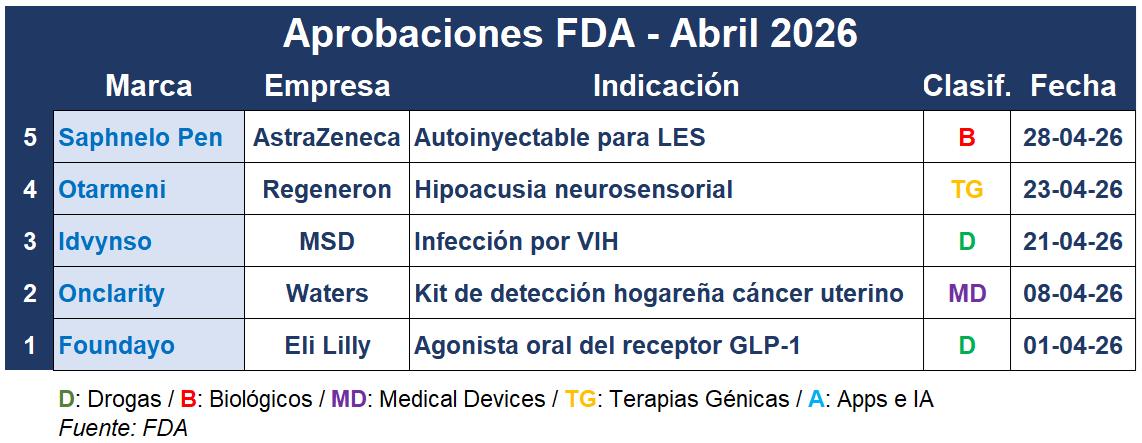
En el arranque de abril la agencia aprobó Foundayo, un agonista del receptor GLP-1 de la norteamericana Eli Lilly para el tratamiento de la obesidad. Esta resulta ser la primera molécula nueva aprobada bajo el programa de Prioridad Nacional, y le mata el invicto a Wegovy de la danesa Novo Nordisk, en tanto al momento, la única agonista oral del receptor GLP-1 para la obesidad. Ver FDA: OK para Foundayo
En paralelo, la norteamericana MSD dio un nuevo paso en el campo del VIH. La multi recibió el OK de la FDA para Idvynso, un régimen combinado de administración diaria que introduce por primera vez en el mercado un nuevo tipo de antirretroviral innovador para ciertos pacientes. Ver luz verde para Idvynso
También en abril, Otarmeni de la estadounidense Regeneron fue avalado por la FDA bajo el programa de Prioridad Nacional, lo cual se informó el mismo día en que la multi dio a conocer un acuerdo de precios con el presidente Donald Trump. Esta se constituye en la primera terapia génica para el tratamiento de la pérdida auditiva. Ver FDA: OK para Otarmeni
Y la FDA aprobó una versión autoinyectable de Saphnelo, el anticuerpo monoclonal de la británica AstraZeneca indicado para el tratamiento del lupus eritematoso sistémico. Saphnelo Pen demostró tener el mismo perfil de seguridad que la versión intravenosa. Ver OK para Saphnelo Pen
Por otro lado se autorizó el uso del Onclarity HPV Self-Collection Kit de la estadounidense Waters para la detección del cáncer de cuello uterino. El mismo está indicado para utilizarse en conjunto con Onclarity HPV Assay de la norteamericana BD. Ver FDA avala test hogareño
Además, durante abril la FDA realizó una serie de anuncios sobre la gestión de la agencia y sus objetivos. Por un lado comunicó que cumplió con las metas que se planteó en el denominado Año 1 y en pos de reducir el uso de animales en el desarrollo de fármacos. Esto en el marco del programa lanzado en el 2025 bajo el nombre de Reducción de las Pruebas con Animales en los Estudios de Seguridad Preclínica. Ver FDA: news en testeos en animales
Por otro lado, las terapias de reemplazo de testosterona apuntan a expandirse bajo una nueva iniciativa de la FDA. La agencia dijo que los tratamientos actualmente aprobados para hombres con niveles bajos de testosterona debido a una causa estructural o genética conocida, podrían tener potencial para casos donde la causa se desconoce. Ver news en terapias de testosterona
El presidente Donald Trump firmó en abril una orden ejecutiva que instruye a la FDA a agilizar la revisión de productos que contienen sustancias psicodélicas. A su vez, destinará fondos federales a la investigación del uso de la ibogaína. Esta medida ya está en plena aplicación, con menos de un mes entre su anuncio y el de las primeras tres empresas seleccionadas para el programa. Ver revisión de psicodélicos | Ver FDA: prioridad para psicodélicos
Y siguiendo en esta línea, se develó un nuevo programa piloto de la FDA que busca reducir las demoras en los ensayos clínicos y acortar los plazos de aprobación para los medicamentos. Ya se comenzaron pruebas de concepto con los laboratorios AstraZeneca y Amgen utilizando señales agregadas en lugar de datos brutos de los pacientes. Ver FDA: clinical trials en tiempo real