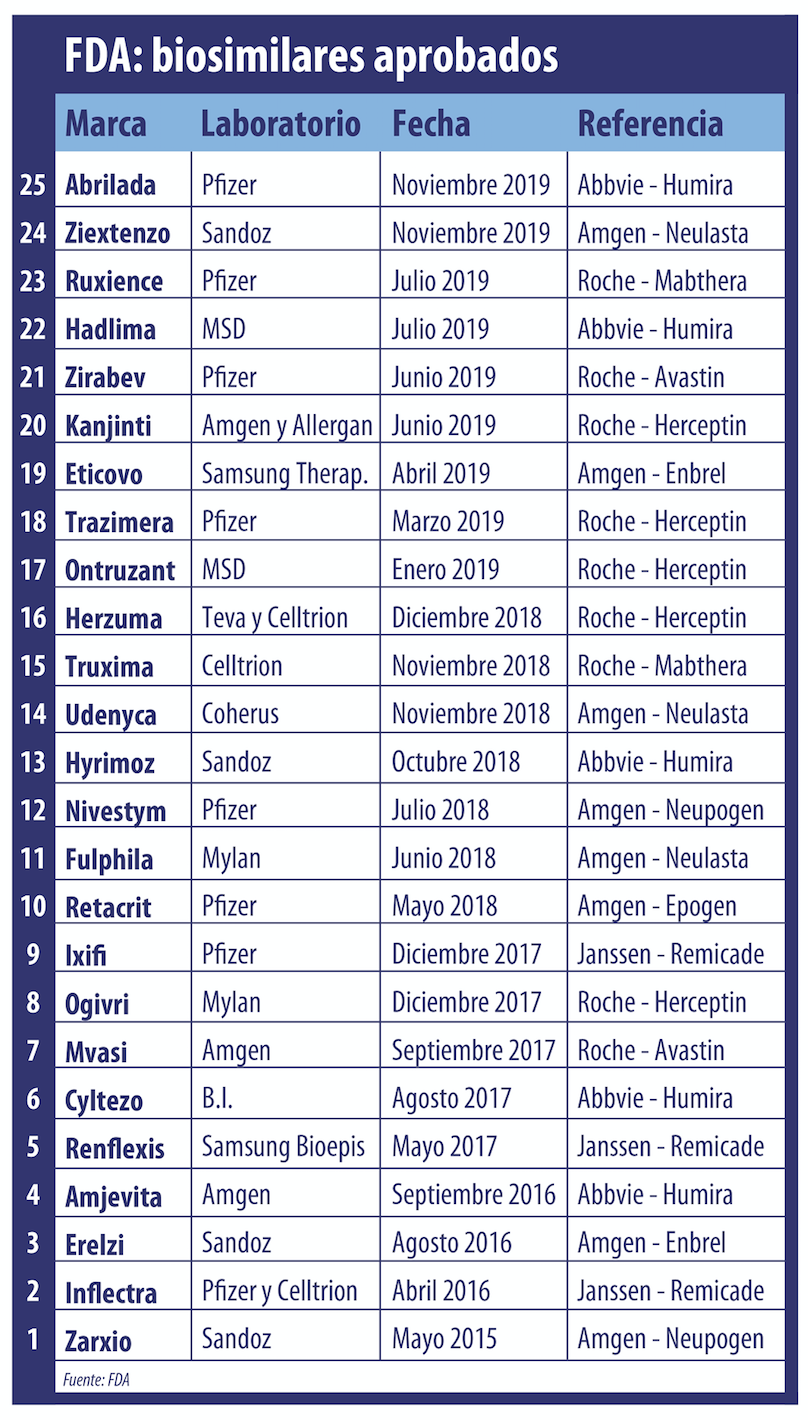
La FDA le puso primera a un nuevo biosimilar de Humira. Se trata del quinto bio del producto insignia de Abbvie, y al que Pfizer bautizó Abrilada. Ahora empató a Herceptin, de Roche, que también suma cinco versiones en los Estados Unidos.
La escalada de biosimilares de Humira no para. El viernes pasado la FDA aprobó Abrilada de la norteamericana Pfizer. Ver Press Release.
De esta forma el nuevo producto se convirtió en el quinto bioequivalente de Humira, la terapia insignia de la norteamericana Abbvie. Esto demuestra además la carrera de Pfizer en el segmento de los biosimilares, ya que Abrilada se constituye en el octavo bio de la multi en ser autorizado por el organismo. Ver comunicado.
La corporación informó que el lanzamiento del medicamento, indicado fundamentalmente en artritis reumatoidea, se proyecta en los Estados Unidos para el 2023 en función de ciertos acuerdos sellados con Abbvie. Este año además fue aprobado Hadlima, de MSD, el cuarto biosimilar de Humira en ese mercado. Ver artículo.