En los meses de agosto y septiembre la FDA aprobó dos nuevos biosimilares. Se trata de Erelzi, propiedad de la multi Sandoz; y Amjevita, de Amgen.
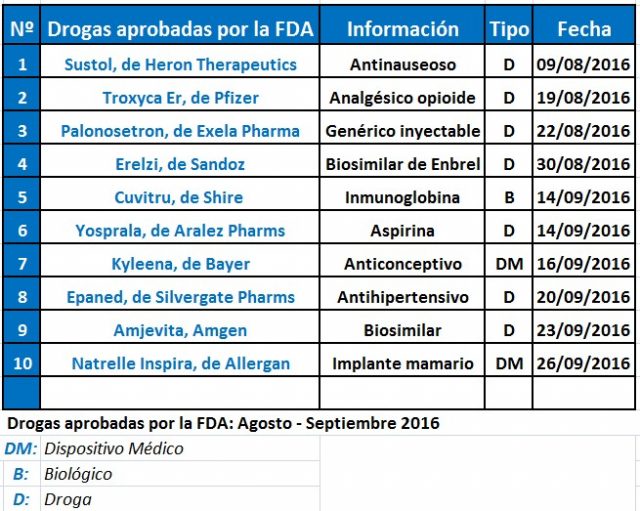
Pharmabiz llevó a cabo un exhaustivo relevamiento sobre los productos clave que la FDA aprobó durante el bimestre comprendido entre agosto y septiembre pasados.
Entre ellos resaltaron un dúo de biosimilares que se convirtieron en nota de tapa. En el mes de agosto, la suiza Novartis a través de su división de genéricos Sandoz recibió el OK para Erelzi, un biosimilar de Enbrel, perteneciente a Amgen. El producto está indicado para condiciones inflamatorias incluyendo la artritis reumatoidea y la psoriasis en placa. Ver artículo
Bayer recibió la aprobación de Kyleena, un nuevo anticonceptivo que consiste en un dispositivo en forma de T fabricado con plástico flexible.
Un mes después, el organismo le levantó el pulgar al biosimilar de Humira, de la biotecnológica Abbvie. El producto fue bautizado como Amjevita y está bajo el paraguas de Amgen. Ver artículo
En el reporte bimestral, otra que sobresalió fue la norteamericana Pfizer, quien obtuvo el aval para su analgésico opioide Troxycaer. Ver press release
Otro producto que saldrá al ruedo gracias a la reciente venia de la FDA será Kyleena, un nuevo anticonceptivo de la alemana Bayer. Se trata de un dispositivo en forma de T fabricado en plástico flexible. Ver artículo
La FDA también le concedió el aval a un producto de Shire. Se trata de Cuvitru, una inmunoglobina subcutánea, para tratar la inmunodeficiencia humoral primaria.
Dos días antes, la FDA le había dado respaldo a una nueva inmunoglobina subcutánea de Shire. Se trata de Cuvitru, indicada para el tratamiento de la inmunodeficiencia humoral primaria. Ver artículo
En materia de medical devices, el dispositivo high tech, MiniMed 670G dio la nota. El innovador producto de la irlandesa Medtronic fue dado a conocer como un dispositivo que opera como un “páncreas artificial”. El novedoso sistema mide el nivel de glucosa en sangre de forma automática cada cinco minutos. Luego, a través de algoritmos deduce y suministra la dosis de insulina que el paciente necesita. Ver artículo
Los dispositivos médicos tuvieron protagonismo en el bimestre. La FDA aprobó dos devices para diabetes pertenecientes a Medtronic y Abbott. Además, Allergan recibió el OK para un nuevo implante mamario.
Otro dispositivo que alcanzó el sí fue FreeStyle Libre Pro, de la norteamericana Abbott. Este sensor se coloca en la parte alta del brazo del paciente, y monitorea constantemente los niveles de glucosa, por hasta 14 días. Ver artículo
Casi al cierre del mes, la irlandesa Allergan logró el OK para su nuevo implante de mamas, Natrelle Inspira Cohesive. El device es una combinación de su ya existente Natrelle Inspira y un gel altamente cohesivo. Las prótesis aprobadas vienen en dos presentaciones: suave y “Biocell”. Ver artículo
Otros laboratorios que obtuvieron el visto bueno de la FDA fueron Heron Therapeutics para el antinauseoso Sustol; Exela Pharma que recibió el aval para Palonosetron Hydrochloride, un genérico inyectable para tratamientos de quimioterapia; y Silvergate Pharms, para su antihipertensivo Epaned.