El 2016 se luce como un año prometedor para las moléculas nóveles. En los primeros tres meses del 2016 la FDA ya le dio el OK a 22 nuevos principios activos.
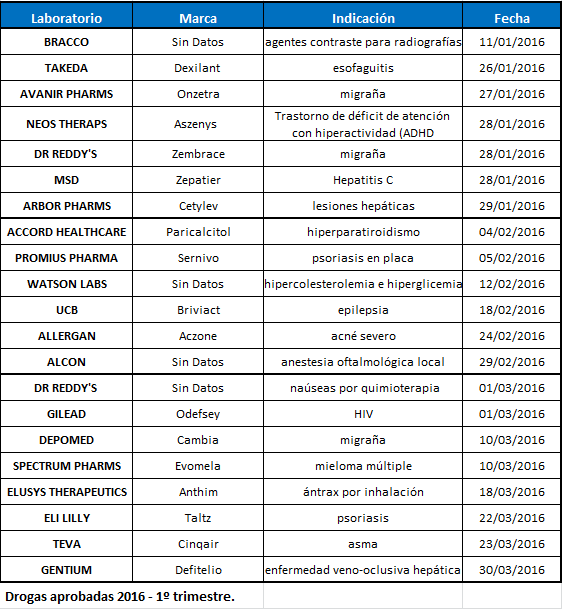
El 2015 fue un año con récord de nuevas moléculas, a través de 45 aprobaciones. Pero parece que el 2016 no se va a quedar atrás. De hecho, en el primer trimestre del año la FDA ya le dio el OK a 21 nuevas entidades moleculares y medicamentos biológicos. Ver listado
Las empresas estrellas del trimestre fueron las norteamericanas MSD, Eli Lilly y Gilead; la japonesa Takeda; la isrealí Teva; la irlandesa Allergan; y la suiza Alcon que forma parte del consorcio Novartis.
Algunas de las empresas ganadoras en el primer trimestre fueron las norteamericanas MSD, Eli Lilly, y Gilead; la japonesa Takeda; la israleí Teva; y la irlandesa Allergan.
En enero, MSD consiguió el OK para Zepatier, indicado para la Hepatitis C. En ese mismo mes, la japonesa Takeda obtuvo el visto bueno para Dexilant, para tratar la esofaguitis. Ver artículo
En febrero, la irlandesa Allergan recibió el OK para Aczone, prescripto para acné severo. Alcon, en tanto, consiguió la aprobación de una anestesia oftalmológica local.
En marzo, las ganadoras fueron Eli Lilly, Gilead y Teva. Lilly, sumó a Taltz, su primer producto para la psoriasis. Teva, en tanto, obtuvo el OK para Cinqair, para el asma; y Gilead, para Odefsey, indicado para el HIV. Ver artículo
La hepatitis C sigue estando en el centro de la escena de farma. En este trimestre se aprobó Zepatier de MSD. La psoriasis es otra estrella, Eli Lilly y Promius obtuvieron el OK para productos indicados para esta enfermedad.
Otras empresas menos populares que consiguieron aprobaciones fueron la norteamericana Arbor, que se hizo de Cetylev, indicado para prevenir lesiones hepáticas; Avanir recibió el visto bueno para Onzetra, para la migraña; y Dr. Reddy para el antimigrañoso Zembrance. A la belga UCB le validaron a Briviact, para la epilepsia.
La india Promius alcanzó el visto bueno para Sernivo, para casos de psoriasis y Gentium para Defitelio, para la enfermedad veno-oclusiva hepática. Spectrum sumó a Evomela, para el mieloma múltiple; Depomed a Cambia, indicado para migraña. Elusys obtuvo la aprobación de Anthim, para el ántrax por inhalación; y Dr. Reddy’s para una inyección a base de palonosetrón para prevenir naúseas durante tratamientos con quimoterapia.
Así en enero, el organismo regulador de Estados Unidos le dio el visto bueno a siete nuevos productos. En el segundo mes del año recibieron la aprobación de la FDA seis. Mientras que en marzo los que alcanzaron el Sí fueron ocho principios activos.