En este marzo de 2021, la CONETEC puso la lupa sobre una decena de tecnologías sanitarias. El organismo publicó una serie de informes en los que se evaluaron oncológicos, anticoagulantes y dispositivos médicos. Para tres productos no se recomendó su cobertura, mientras que para seis se sugirió una cobertura condicional sujeta a determinados requisitos. Sólo un device consiguió luz verde por parte de la mesa técnica de la comisión.
Los medicamentos de nueva generación implican constantes cuestionamientos en torno a la relación costo/beneficio de incluirlos en la cobertura por parte de la seguridad social. Y es en este sentido que la CONETEC -la Comisión Nacional de Evaluación de Tecnologías de Salud- se expidió sobre una decena de productos.
El organismo, que tomó forma en el 2018, publicó ocho informes de evaluación con fecha de marzo de este 2021. Allí analizó principalmente oncológicos, así como tres anticoagulantes y dos dispositivos médicos.
Por caso, la CONETEC puso la lupa sobre Venclexta, que lleva el sello de la norteamericana Abbvie y la suiza Genentech -del grupo Roche- y que tiene un precio de $205.229,63 (u$s 2.1 mil) mensuales . Fue para evaluar su uso en el tratamiento de la leucemia mieloide aguda. La mesa técnica consideró que su cobertura «probablemente genere un impacto positivo en la salud pública». Sin embargo, recomendó no cubrir el producto en el marco actual ante «los elevados costos que implica la implementación de la tecnología y la incertidumbre sobre la magnitud de los efectos más allá de los 20 meses». Ver informe nº 15.
Tampoco le otorgó el visto bueno a Herceptin, de Roche, en el tratamiento del cáncer de mama HER2 positivo. El organismo consignó que su uso tendría un impacto neutro en la equidad y probablemente negativo para la salud pública. Además resaltó que «en el contexto actual y ante la existencia de biosimilares» se recomienda no cubrir la tecnología que ronda los $271.172,10 (u$s 2.7 mil). Ver informe nº 14.
En tanto Opdivo, de la norteamericana BMS, fue estudiado como terapia de segunda línea para el cáncer de pulmón de células no pequeñas. En este caso, la CONETEC sugirió una «cobertura condicional, sujeta a la aplicación conjunta de los siguientes términos»: una reducción sensible del precio -que es de $245.685,02 (u$s 2.5 mil) por frasco ampolla de 10 ml-; y que la indicación apunte a una población específica, de acuerdo a la expresión de ciertos marcadores tumorales. Ver informe nº 10.
El organismo dio una respuesta similar para el uso de Keytruda, de MSD, en primera línea para melanoma avanzado, metastásico o irresecable, sin mutación BRAF. Recomendó una cobertura condicional de este tipo de productos, catalogados como agentes anti PDL-1. Es en función de que se aplique una disminución del precio -que es de $454.523,40 (u$s 4.6 mil) por frasco ampolla-; que se use la opción más económica entre las disponibles; y que la cobertura sea específica de acuerdo a la condición clínica de la persona. Ver informe nº 13.
En simultáneo la CONETEC se expresó sobre Mekinist junto con Tafinlar, ambos de la suiza Novartis, para el tratamiento adyuvante del melanoma resecado con mutación BRAFV600. Dijo que «puede sugerirse una cobertura condicional«. Esto en función no sólo de una reducción en su precio y una indicación específica, sino también sujeto a que «el tratamiento puede continuar hasta la reaparición de la enfermedad, la toxicidad inaceptable o hasta un máximo de 12 meses». Los productos en conjunto implican un desembolso de $1.226.287,9 (u$s 12.6 mil). Ver informe nº 12.
Por otro lado, en un mismo documento se analizaron tres anticoagulantes orales de acción directa (ACOD) en casos de fibrilación auricular no valvular. Son Eliquis, de la norteamericana Pfizer, que cuesta $10.916,62 (u$s 112); Pradaxa, de Boehringer Ingelheim, con un precio de hasta $13.826,61 (u$s 142); y Xarelto, de Bayer, que ronda los $9.848,57 (u$s 101). En el informe la CONETEC también recomendó una cobertura condicional sujeta a que el 40% del gasto devenga del financiador; y a que la indicación sea otorgada por especialistas registrados y con adecuada experiencia en el manejo de personas anticoaguladas; entre otros factores. Ver informe nº9.
Además el organismo evaluó los sistemas de infusión continua de insulina con sensor de glucemia, en personas con diabetes mellitus tipo 1. Para ellos no recomendó su cobertura debido a que «tendría un impacto probablemente negativo sobre la equidad y para la salud pública». Ver informe nº 16.
Por último, los que sí obtuvieron luz verde por parte de la entidad fueron los test de VPH en estrategia de screening primario para la detección del cáncer cervicouterino. La mesa técnica recomendó cubrir la tecnología «con la existencia de normativas de entidades nacionales que avalan esta estrategia». Además agregó que «la posibilidad de contar con dispositivos que garanticen el método de auto-toma de muestras podría incluso mejorar la equidad en el acceso y los resultados globales de la estrategia de diagnóstico». Ver informe nº 11.
La CONETEC emite recomendaciones a la autoridad sanitaria sobre la incorporación, forma de uso, financiamiento y políticas de cobertura de las tecnologías sanitarias desde una perspectiva global del sistema de salud argentino. Ver sitio.
u$s 1 = $ 97,10 (Cotización BCRA al lunes 22/03/2021 – 15hs)
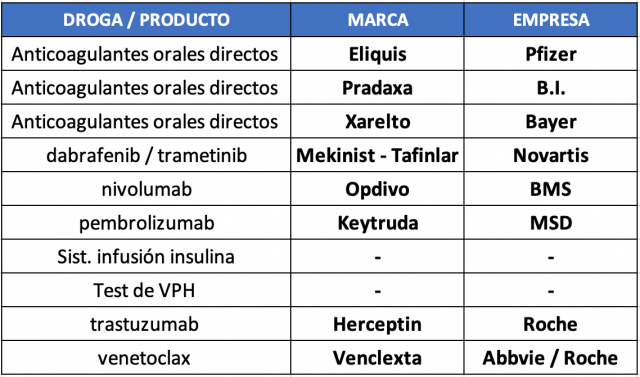

Las CONETEC evaluó ocho tecnologías. Mira el informe. #CONETEC #Medicamentos #DispositivosMédicos #TecnologíasSanitarias #Cobertura #Farma #Pharmabiz














