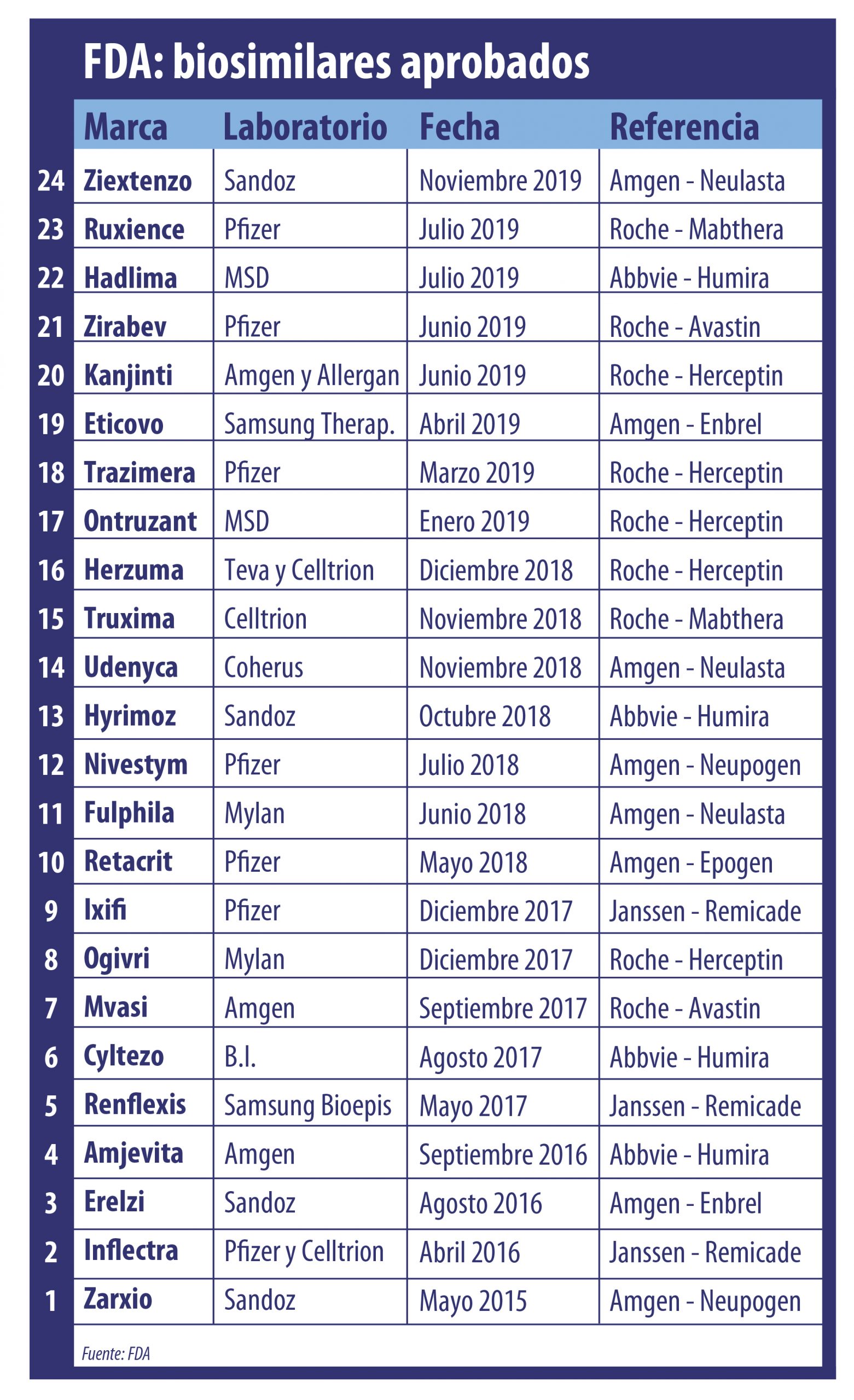
La FDA alcanzó los 24 biosimilares aprobados. Fue luego de darle el visto bueno a Ziextenzo de Sandoz, el que toma como referencia a Neulasta, de Amgen.
Los biosimilares están en la agenda regulatoria a nivel global. Ahora la FDA le levantó el pulgar a un nuevo producto de este tipo y ya suma un total de 24 aprobados. Ver infografía.
Esta semana la agencia regulatoria le dio luz verde a Ziextenzo, en base a pegfilgrastim, el que lleva el sello de Sandoz, la división de genéricos de la suiza Novartis. El mismo se constituyó en el tercer bioequivalente de Neulasta, de la norteamericana Amgen. Ver press release.
El medicamento, que además es el cuarto biosimilar de Sandoz en obtener el OK por parte de la FDA, fue avalado para disminuir la incidencia de neutropenia febril, uno de los efectos secundarios de la quimioterapia.
Ziextenzo ya se comercializa en Europa, tras haber sido autorizado por la EMA en noviembre del 2018. Según lo detallado por Sandoz, el producto sería lanzado en los Estados Unidos durante este año. Ver artículo.