La FDA le levantó el pulgar a una droga con sello argentino. Se trata de benznidazol el medicamento para tratar la Enfermedad de Chagas, propiedad del Grupo Chemo, de Hugo Sigman.
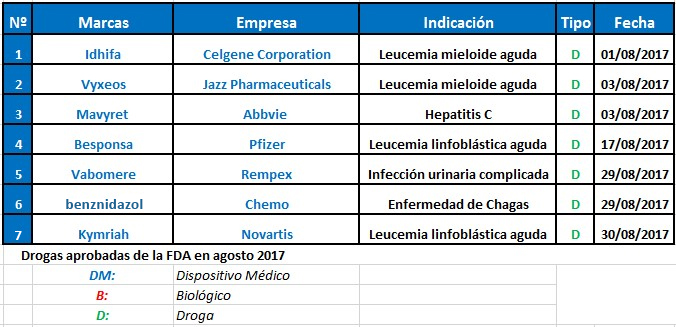
Pharmabiz realizó un relevamiento de las moléculas que aprobó la FDA durante el mes de agosto.
El hecho destacado del mes llegó de la mano de una droga con sello argentino. Se trata de benznidazol, el medicamento utilizado para tratar la Enfermedad de Chagas, del Grupo Chemo, propiedad del empresario Hugo Sigman. El producto, que se comercializa en la Argentina desde hace más de una década, recibió el OK de la FDA y es el primer tratamiento aprobado en los Estados Unidos para esta enfermedad. Ver artículo.
La saga de productos para la hepatitis tuvo una nueva versión durante el mes de agosto. Esta vez la noticia la dio Abbvie que recibió la venia del organismo para Mavyret.
Por otro lado, la norteamericana Abbvie obtuvo el aval del organismo para Mavyret, el primer tratamiento para la hepatitis C que tiene ocho semanas de duración -el standard era de 12 semanas-. El medicamento está indicado en pacientes adultos sin cirrosis o con cirrosis leve. Ver artículo.
Los oncológicos también dieron la nota durante agosto. La FDA le dio luz verde a Besponsa, de la norteamericana Pfizer, para el tratamiento de la leucemia linfoblástica aguda refractaria en adultos. En la misma línea, la agencia regulatoria aprobó Kymriah, de la suiza Novartis. Se trata de la primera terapia génica basada en células para tratar este tipo de leucemia. Ver artículo. Ver artículo.
Los oncológicos también dieron la nota. La FDA le dio luz verde a Besponsa, de Pfizer; y a Kymriah, de Novartis; ambos indicados para tratar la leucemia linfoblástica aguda.
En tanto, Celator Pharma -subsidiaria de la irlandesa Jazz Pharmaceuticals-, fue otra de las firmas que consiguió el OK del organismo regulatorio de los Estados Unidos. Fue para Vyxeos, un inyectable destinado a tratar dos tipos de leucemia mieloide aguda en adultos. El producto recibió a su vez la designación de medicamento huérfano. Ver artículo.
Otra empresa que contó con el respaldo de la FDA fue la biotecnológica Celgene, con Idhifa. La nueva molécula, desarrollada junto con Agios Pharmaceuticals, apunta a tratar también la leucemia mieloide aguda refractaria en pacientes adultos. Ver press release.
Por último, la norteamericana Rempex obtuvo el aval de la agencia durante este mes. Fue para Vabomere, su medicamento antibacterial indicado para infecciones urinarias complicadas en adultos. Ver artículo.