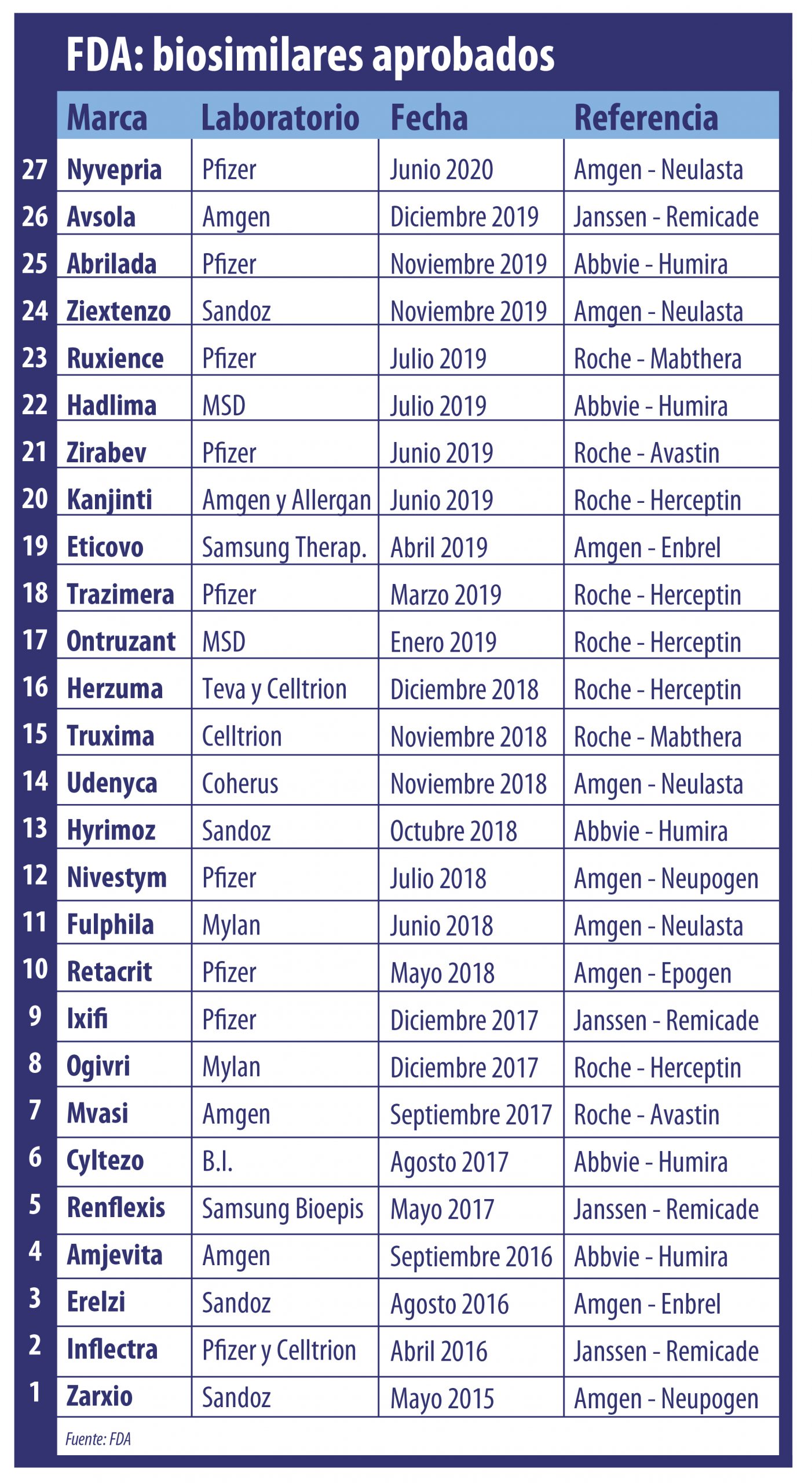
Hoy la FDA avaló el primer biosimilar de este 2020 alcanzando las 27 aprobaciones de este tipo. Lo nuevo en Estados Unidos es Nyvepria de la norteamericana Pfizer, el cuarto bio del oncológico Neulasta propiedad de la norteamericana Amgen.
En este junio de pandemia, la FDA aprobó el primer biosimilar del año. El aval fue para Nyvepria de la norteamericana Pfizer. Ver press release.
De esta forma, el producto se convierte en el cuarto bioequivalente del oncológico Neulasta, el que lleva el sello de la norteamericana Amgen.
Nyvepria competirá con Fulphila de la firma de genéricos Mylan y la india Biocon; con Udenyca de la norteamericana Coherus BioSciences; y con Ziextenzo de Sandoz, la división de genéricos de la suiza Novartis. Ver artículo. Ver artículo.
Así con esta nueva aprobación otorgada por la FDA, la cantidad total de biosimilares autorizados en los Estados Unidos al momento llega a 27. El último aval había sido para Avsola, de Amgen, en diciembre pasado. Ver artículo.