En agosto la FDA estuvo súper activa en materia de aprobaciones. Por caso le dio luz verde a un nuevo medicamento para la tuberculosis, el que fue desarrollado por una ONG. Además le levantó el pulgar a Rinvoq, un producto para la artritis reumatoide que lleva el sello de la norteamericana Abbvie.
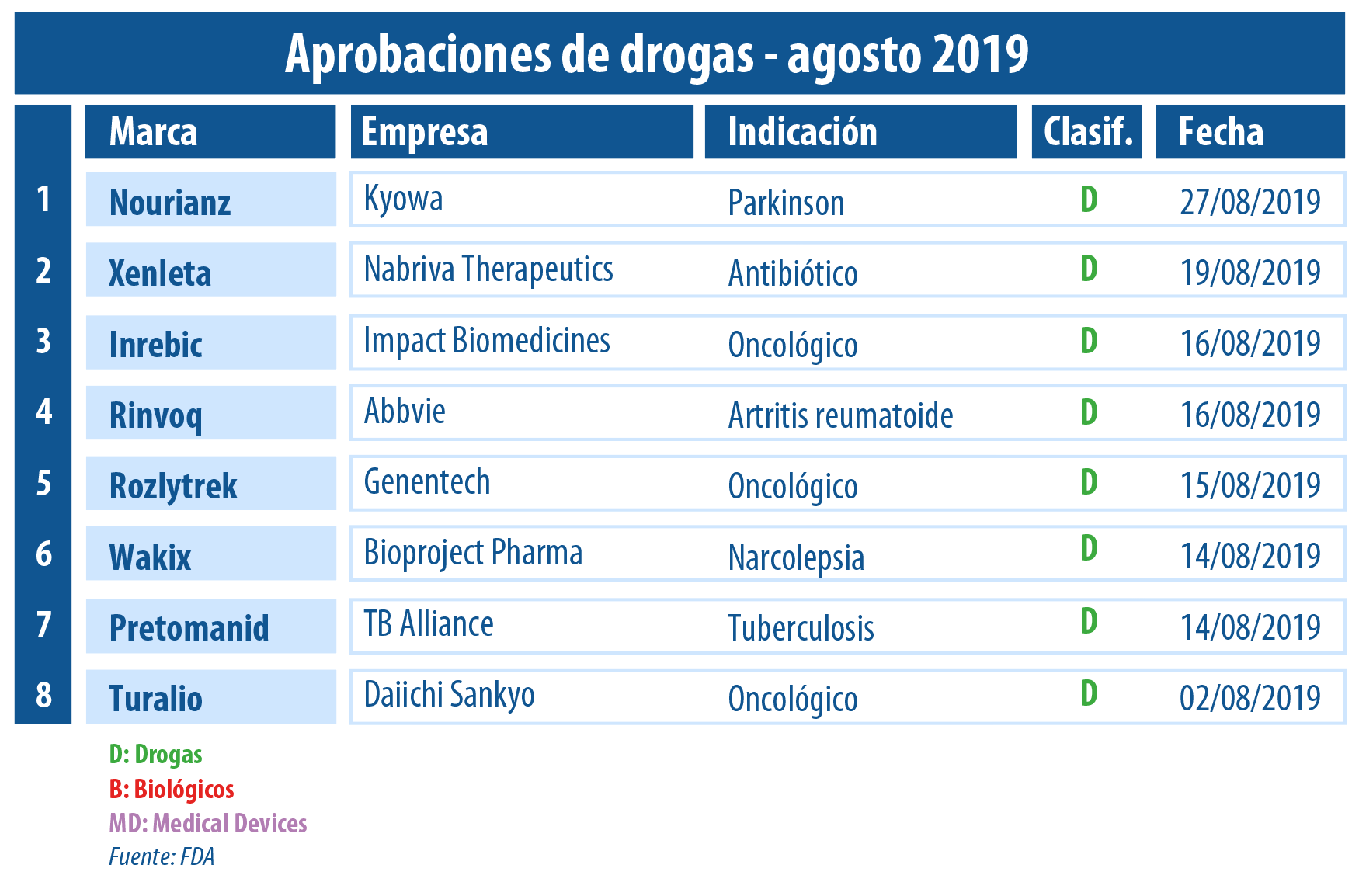
El mes de agosto llegó a su fin y el equipo de Pharmabiz vuelve con su resumen mensual que refleja las principales aprobaciones otorgadas por la FDA en este período.
Por caso se destacó el visto bueno a un nuevo medicamento para la tuberculosis a base de pretomanid. El diferencial es que fue desarrollado por una institución sin fines de lucro, la TB Alliance. El mismo, se constituyó como la tercera droga para dicha enfermedad en ser autorizada en más de 40 años por el organismo. Ver artículo.
Los oncológicos también dieron la nota durante agosto. La biotecnológica Genentech del grupo suizo Roche recibió luz verde para Rozlytrek, a base de entrectinib, el segundo medicamento avalado por la FDA para un tipo específico de cáncer de pulmón. Ver artículo.
A lo largo de este período, los oncológicos también dieron la nota. El organismo avaló a Rozlytrek de la biotecnológica Genentech e indicado para cáncer de pulmón. También autorizó a Turalio, de la japonesa Daiichi Sankyo; y a Inrebic, de la norteamericana Impact Biomedicines.
En paralelo, la japonesa Daiichi-Sankyo obtuvo el OK para Turalio, un oncológico aprobado para adultos con tumores de células gigantes tenosinoviales. A su vez, la agencia regulatoria le levantó el pulgar a Inrebic, el que lleva el sello de la norteamericana Impact Biomedicines y que está indicado para ciertos tipos de mielofibrosis. Ver artículo. Ver artículo.
Por otra parte, el organismo autorizó a Rinvoq, un nuevo producto para artritis reumatoidea que pertenece a la norteamericana Abbvie y que saldrá a competir con Xeljanz, de Pfizer; y Olumiant, de Eli Lilly. Ver artículo.
Otra molécula a la que la FDA le concedió el OK fue Wakix, que está indicado para la somnolencia diurna excesiva en adultos con narcolepsia. El medicamento, que lleva el sello de la francesa Bioproject Pharma, es el primer y único tratamiento avalado para personas con este trastorno, que no está listado como sustancia controlada por la Administración de Control de Drogas, DEA. Ver Press Release.
En el octavo mes del año, la agencia también aprobó al antibiótico Xenleta, de la irlandesa Nabriva Therapeutics, para tratar a adultos con neumonía bacteriana adquirida en la comunidad, es decir no de manera intrahospitalaria. Ver artículo.
Por último, la FDA autorizó a Nourianz, un nuevo producto que lleva el sello de la japonesa Kyowa Kirin y que está indicado como terapia adicional para la enfermedad de Parkinson. Ver Artículo.